12000元獎金池——"雙洳學術論文獎勵計劃"再開啟!
發布時間:
2024-08-15 14:30
2024~2025年“雙洳學術論文獎勵計劃”
為感謝廣大客戶對雙洳生物Lonsera®產品的支持與信任,我們將對使用雙洳生物Lonsera®血清產品并在SCI期刊發表文章的科研工作者給予豐厚獎勵!
此次論文獎勵采取設置獎金池的方式,按向公眾號提交獎勵申請的先后順序進行獎金發放,信息核實后獎勵生效,先到先得。
獎金池設置
總金額:12000元
獎勵群體:使用雙洳生物Lonsera血清產品并在SCI期刊發表文章的科研工作者
有效期:從2024年8月1日至獎金發放完畢為止
獎勵標準
獎勵以官方最新公布的SCI期刊影響因子(IF)數據為準:
| 影響因子 | 獎勵金額 |
| 5<IF<10 | 150元 |
| 10≤IF<15 | 300元 |
| 15≤IF<20 | 600元 |
| 20≤IF<25 | 900元 |
| 25≤IF | 1250元 |
注:若獎勵申請者在申請時可同步提交本篇論文的解析,采納后獎勵金額將增加100%。
(論文解析參照本篇推文末尾“文獻解析分享” )
獎勵說明
購買使用雙洳生物Lonsera®血清產品,在國內外刊物上發表文章,并注明使用產品所屬雙洳生物Lonsera®的國內外科研人員方有權申請獎勵。
注:
(1)使用雙洳生物血清產品在SCI上發表論文,文章中需注明所使用血清的正確名稱以及產品所屬公司名稱:“雙洳生物”簡稱(或Suzhou Shuangru Biotechnology Co., Ltd.)”,并標注該商品所屬品牌“LONSERA”。(可參考下圖)

(2)獎勵第一作者或通訊作者申請(每篇文章僅限申請一次)。
(3)同一申請人若有多篇見刊論文引用同一產品,則按最高影響因子所在檔實施單次最大獎勵,不予重復獎勵。
(4)一篇論文僅獎勵一次,同一論文使用多款產品,不進行獎勵疊加。
(5)接收論文獎勵即表示作者已默認授權雙洳生物使用論文用于產品宣傳和品牌推廣。
(6)獎勵采取“先到先得”的方式,直到獎金池內的資金發放完畢為止。一旦獎金池內的資金發放完畢,獎金池即刻關閉,不再接受新的申請。
(7)僅限 2024年8月1日起發表的學術論文,以見刊時間為準,獎勵參照最新公布的影響因子數據。
(8)活動有效期至獎勵金額發放完畢(共計12000元),蘇州雙洳生物科技有限公司享有活動最終解釋權。
(9)獎金金額由雙洳生物公司代扣代繳個稅后直接發放到個人。
參與方式
1、在線填寫雙洳生物Lonsera®文獻獎勵申請表單(見二維碼);或于雙洳生物公眾號回復“論文獎勵”,掃碼填寫并提交相關信息;
2、雙洳生物收到申請后,5個工作日內完成審核;
3、審核通過后,將于15個工作日內發放獎金。
 申請獎金掃碼填寫
申請獎金掃碼填寫
文獻解析分享

文獻引用產品:Lonsera ® FBS
文獻引用產品貨號:S711-001S
影響因子(IF)=38.3
第一作者名稱:高金超
通訊作者名稱:高小玲
作者單位:上海交通大學醫學院
發表時間:2023-12-29
研究方向:腦內遞送,納米遞送系統
 掃碼查看文獻原文
掃碼查看文獻原文
01 論文標題
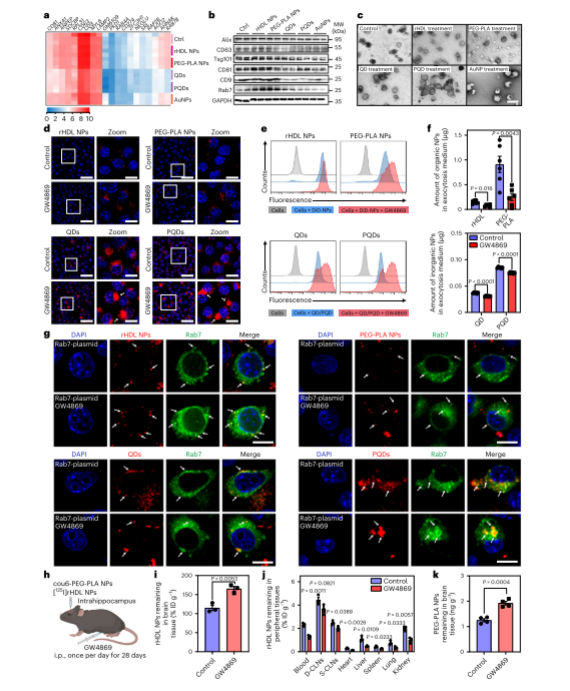
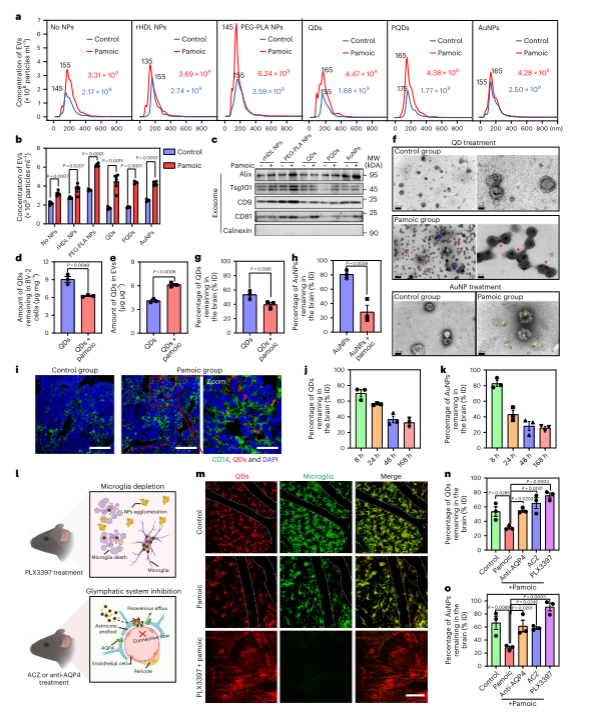
Intracerebral fate of organic and inorganic nanoparticles is dependent on microglial extracellular vesicle function
腦內有機和無機納米顆粒的命運取決于小膠質細胞外囊泡的功能
02 論文摘要
納米粒子(NPs)代表了通過血腦屏障傳遞診斷和治療藥物的重要進展。然而,NP清除對安全性和治療適用性至關重要。在這里,我們報告了從大腦中清除模式有機和無機NPs的研究。我們發現小膠質細胞外囊泡(ev)在清除腦內無機和有機NPs中起著至關重要的作用。與有機NPs不同,無機NPs通過抑制ERK1/2信號傳導干擾小膠質細胞ev的生物發生。這增加了無機NPs在小膠質細胞中的積累,阻礙了它們通過血管旁途徑的消除。我們還證明,通過ERK1/2激活劑刺激小膠質細胞ev的釋放,可以增加血管旁淋巴通路介導的腦對無機NPs的清除。這些發現強調了小膠質細胞ev對大腦中有機和無機NPs清除的不同模式的調節作用,并提供了一種調節NPs腦內命運的策略。
03 結論
在進入大腦后,無機和有機NPs在小膠質細胞中表現出不同的細胞內運輸和胞外分泌行為。與有機NPs (rHDL和PEG-PLA NPs)不同,無機NPs (QDs、PQDs和AuNPs)抑制ERK1/2信號傳導和EV釋放,導致NPs長期滯留在小膠質細胞中,導致NPs無法從大腦中清除。因此,增加小膠質細胞的EV釋放可能成為幫助從大腦中去除納米材料的潛在策略。因此,該研究成功地通過ERK1/2激活劑處理后的小膠質細胞EV釋放提高了無機NPs的腦清除。總的來說,這項工作提供了對NPs在大腦中的命運的洞察,并展示了一種控制工程NPs在大腦內命運的方法。